L’ectopia cordis est une malformation congénitale extrêmement rare, où le cœur se développe à l’extérieur de la poitrine chez un fœtus en développement. Cette condition survient lorsque la cage thoracique ne se forme pas correctement, laissant le cœur sans protection des muscles, de la peau et des os.
Si un fœtus parvient à survivre jusqu’à la naissance, un traitement immédiat pour couvrir le cœur ou tenter de le replacer dans le thorax peut s’avérer vital, bien que ces interventions soient souvent complexes et risquées.
Bien qu’il existe des cas de chirurgie réussie, l’ectopia cordis demeure une condition grave, avec de faibles chances de survie à long terme.
Qu’est-ce que l’ectopia cordis ?
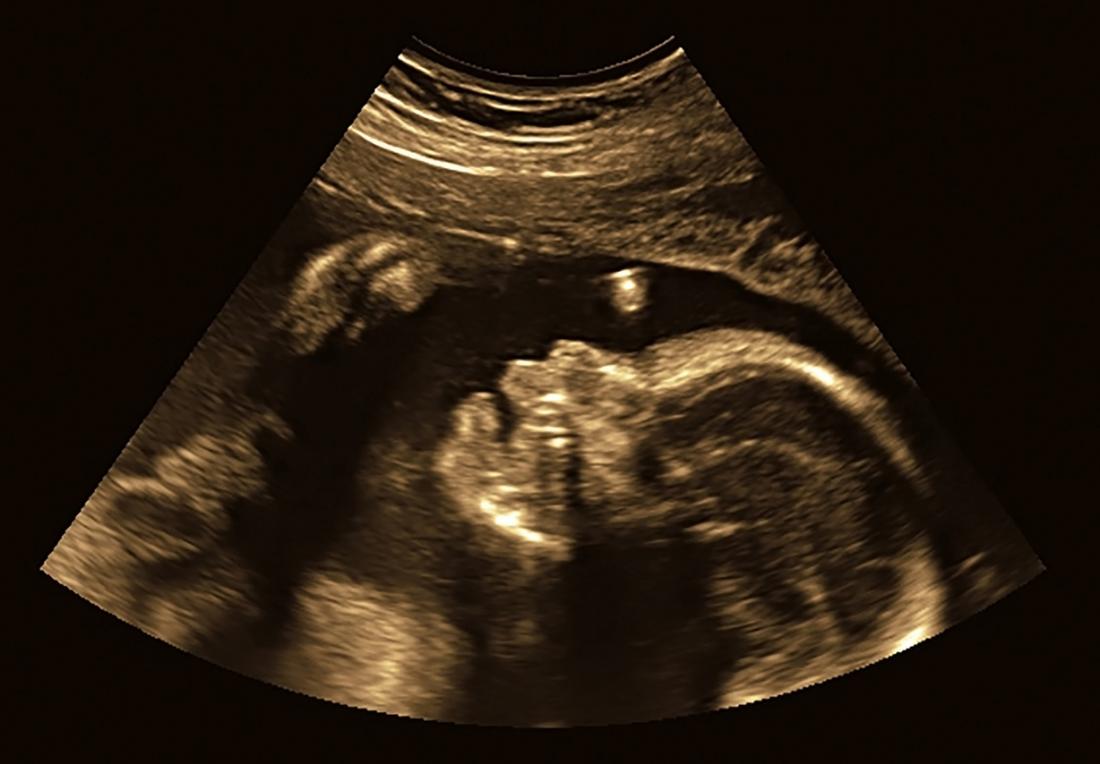
Le terme « ectopie » désigne une position anormale d’un organe, tandis que « cordis » provient du latin et signifie cœur. Ainsi, l’ectopia cordis se manifeste lorsque le cœur ne se situe pas à l’endroit approprié dans le corps.
Cette malformation se produit dans environ 5,5 à 7,9 naissances par million. Au fur et à mesure que le fœtus se développe, le cœur peut apparaître en dehors de la cavité thoracique, soit partiellement, soit complètement.
Il existe quatre positions principales où le cœur peut se développer chez un bébé atteint d’ectopia cordis :
- dans 60 % des cas, le cœur est situé immédiatement à l’extérieur de la poitrine;
- dans 15 à 30 % des cas, il se développe en ligne avec le ventre;
- dans 7 à 18 % des cas, il est positionné entre la poitrine et le ventre;
- dans moins de 3 % des cas, il se trouve en ligne avec le cou.
Quelles sont les causes de l’ectopia cordis ?
Les recherches concernant les causes de l’ectopia cordis sont encore en cours. Étant une malformation congénitale, elle se développe dans l’utérus et est présente dès la naissance.
Le sternum, un os plat qui relie les côtes et forme la partie antérieure de la cage thoracique, joue un rôle clé dans la protection du cœur et des poumons. Si le sternum ne se développe pas correctement pendant la grossesse, le cœur peut se retrouver à l’extérieur du thorax, sans protection.
De plus, cette condition peut être associée à un phénomène rare connu sous le nom de pentalogie de Cantrell, où d’autres organes, comme le diaphragme et la paroi abdominale, ne se développent pas correctement.
Diagnostic

Le cœur du fœtus commence à se former très tôt dans la grossesse, et les os de la cage thoracique se développent peu après. Le rythme cardiaque devrait être régulier dès les premières semaines de la grossesse, et la cage thoracique se complétera pour protéger le cœur durant le premier trimestre.
Les échographies pratiquées lors des premiers stades de la grossesse permettent généralement de détecter l’ectopia cordis. Si cette malformation n’est pas identifiée durant la grossesse, elle sera évidente à la naissance.
Une détection précoce des anomalies de développement offre de meilleures perspectives de traitement, car cela permet aux médecins de préparer des soins d’urgence dès la naissance.
Le traitement est-il possible ?
Le taux de survie pour les bébés atteints d’ectopia cordis est d’environ 10 %, et la plupart des cas se traduisent par des mortinaissances. Malheureusement, les nourrissons qui survivent à la naissance font souvent face à des décès dans les heures ou jours qui suivent.
La détection précoce de la maladie peut être un atout. Si le cœur est par ailleurs en bonne santé, les chances de succès thérapeutique sont considérablement améliorées.
Étant donné qu’un cœur exposé n’a aucune protection contre les infections ou les blessures, le traitement doit commencer immédiatement après la naissance. Le nourrisson sera généralement placé sous ventilation mécanique pour assurer un apport en oxygène adéquat, car il peut avoir des difficultés à respirer seul.
Si l’espace le permet, les chirurgiens réaliseront une opération d’urgence pour replacer le cœur dans la cavité thoracique. Cependant, dans de nombreux cas, le cœur est positionné de telle manière qu’il doit être recouvert d’une greffe de peau ou d’un bouclier cardiaque externe.
Étant donné que l’ectopia cordis survient souvent en association avec d’autres malformations, les chirurgiens peuvent également être amenés à effectuer des interventions correctives supplémentaires à ce stade.
Il est probable qu’un nouveau-né présentant cette condition doive passer une période prolongée à l’hôpital, où des médecins surveilleront attentivement son état de santé et son développement. D’autres traitements et interventions chirurgicales seront probablement nécessaires.
Complications
Les nourrissons survivants à l’ectopia cordis peuvent présenter des cœurs moins robustes que ceux des autres enfants, ce qui peut limiter leur capacité à participer à des activités physiques intenses. De plus, des problèmes de développement mental peuvent survenir.
Ces enfants pourraient également nécessiter une assistance respiratoire, en plus de faire face à d’autres problèmes médicaux, en raison des malformations cardiaques souvent associées. Les interventions chirurgicales postérieures, comme la fermeture de la cavité thoracique, peuvent comporter des risques significatifs.
Cas de survie
Une étude menée en 2017 a examiné 17 cas d’ectopia cordis dans deux centres médicaux entre 1995 et 2014. Elle a révélé que six enfants âgés de 1 à 11 ans avaient survécu, bien que deux d’entre eux aient nécessité une assistance respiratoire par ventilation.
Un article du Texas Children’s Hospital en 2013 relate l’histoire d’un bébé né avec cette malformation qui a survécu à la chirurgie et a célébré son premier anniversaire, avec un bouclier externe protégeant son cœur, prévu pour être remplacé par une protection interne lorsque cela sera possible.
Une étude de 2015 sur un garçon de 11 ans ayant subi une intervention chirurgicale réussie pour couvrir son cœur à la naissance a montré qu’il avait une qualité de vie généralement bonne et qu’il pouvait participer à des activités sportives tout en fréquentant une école pour enfants ayant des besoins particuliers.
Avec les avancées de la médecine, les professionnels de santé espèrent que le taux de survie continuera à s’améliorer.
Perspective
Un scanner néonatal réalisé au cours des 12 premières semaines de grossesse est essentiel pour détecter des malformations congénitales comme l’ectopia cordis. Si un choix est fait d’interrompre la grossesse, il est crucial qu’un professionnel de la santé apporte un soutien et des conseils impartiaux sur l’avortement.
Les femmes enceintes peuvent également opter pour des soins palliatifs ou une intervention chirurgicale immédiate après la naissance, selon la gravité des anomalies cardiaques détectées. Cette décision peut être influencée par la gravité des défauts observés avant ou après la naissance.
L’ectopia cordis est souvent associée à une mortinatalité ou à la mort néonatale. Des organisations comme l’American Pregnancy Association offrent un soutien émotionnel et des conseils aux familles durant cette période éprouvante.
Survivre à l’ectopia cordis implique de surmonter de nombreux défis, notamment des interventions chirurgicales et des soins médicaux continus. Cependant, les options de recherche et de traitement progressent constamment, offrant de l’espoir pour un avenir meilleur aux enfants diagnostiqués avec cette condition.
Nouvelles Perspectives de Recherche en 2024
L’année 2024 marque un tournant dans la compréhension et le traitement de l’ectopia cordis. Des recherches récentes ont mis en lumière de nouvelles techniques d’imagerie prénatale, permettant une détection encore plus précoce de cette malformation. Cela pourrait contribuer à une prise en charge plus efficace, augmentant ainsi les chances de survie des nourrissons concernés.
Des études cliniques en cours examinent également l’utilisation de biomatériaux pour le traitement chirurgical du cœur exposé, offrant une alternative prometteuse aux greffes de peau traditionnelles. Les résultats préliminaires indiquent que ces matériaux pourraient non seulement protéger le cœur, mais aussi favoriser une meilleure intégration avec les tissus environnants.
Enfin, la recherche sur les facteurs génétiques impliqués dans l’ectopia cordis progresse, ouvrant la voie à des approches préventives et personnalisées. Cela pourrait potentiellement aider à identifier les familles à risque et à leur offrir des conseils génétiques adaptés.








